Gynécologie générale
Publié le 31 mar 2008Lecture 10 min
HPV : quand demander un génotypage ?
Le génotypage désigne l’analyse moléculaire de l’ADN viral permettant d’identifier les différents génotypes de papillomavirus humains (HPV) présents dans un échantillon biologique.
L’intérêt de la détection des HPV en agrégat de 13 HPV à haut risque a été largement démontré, en particulier dans le tri des frottis ASC-US, dans la surveillance post-traitement des lésions de haut grade, mais également en dépistage primaire.
Les progrès techniques, qui rendent aujourd’hui possible la réalisation du génotypage à large échelle, posent la question de la place de l’utilisation du génotypage en pratique clinique.
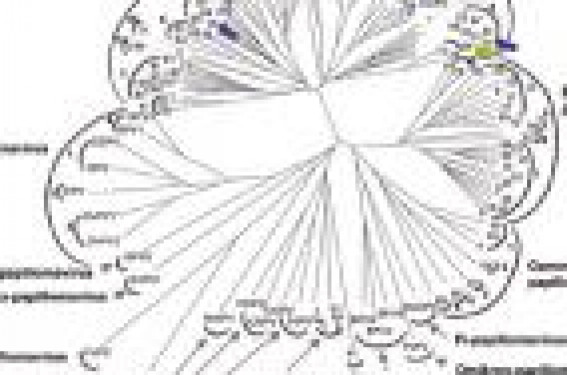
Classification des papillomavirus On observe une grande diversité des papillomavirus (PV) chez les mammifères et les oiseaux. Pourtant, leur génome est stable, peu sujet aux mutations ou aux recombinaisons qui interviennent à la même fréquence que dans le génome de l’hôte. Trente ans de recherches ont été nécessaires pour séquencer et analyser plusieurs centaines d’isolats et établir un système de classification stable qui puisse accepter de nouveaux types de PV. Différents niveaux taxonomiques ont ainsi été définis : famille (Papillomaviridae), genre (alpha, bêta, etc.), espèce (1, 2… ; peu utilisé), type (hôte et numéro : HPV1 pour Human PV, BPV1 pour Bovine PV, etc. ; un type donné possède plus de 10 % de variations de séquence par rapport aux autres PV connus), sous-type (2 à 10 % de variations de séquence), variant (moins de 2 % de variations de séquence), et ont permis d’établir des algorithmes phylogénétiques (figure 1) comparant soit des séquences entières de PV, soit des fragments sub-génomiques. Pour distinguer les différents types de PV entre eux, l’analyse d’un fragment de 291 paires de bases, situé dans L1, est suffisante. Figure 1. Arbre phylogénique des papillomavirus (d’après de Villiers et coll. 2004). Chez l’homme, plus d’une centaine de types ont été isolés, mais c’est le seul hôte qui a été étudié de façon intensive. Pour des raisons pratiques, les PV humains ont été groupés en fonction de leur pouvoir pathogène : d’une part, en fonction de leur tropisme : HPV cutanés ou HPV muqueux ; d’autre part, en fonction de leur potentiel oncogène (concerne uniquement les HPV muqueux) : HPV muqueux à haut risque oncogène (HPV 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73, 82), probablement à haut risque oncogène (HPV 26, 53, 66), à bas risque oncogène (6, 11, 40, 42, 43, 44, 54, 61, 70, 72, 81, 89) et enfin à risque indéterminé (55, 62, 64, 67, 69, 71, 74, 83, 84, 85). Pour rappel, les condylomes acuminés sont dus aux HPV à bas risque ; les lésions de haut grade (précancéreuses) et les cancers, aux HPV à haut risque. Techniques de génotypage Si les techniques évoluent vers toujours plus de sensibilité et de performance, il ne faut pas oublier l’importance de la qualité du prélèvement. Le génotypage des HPV peut être réalisé sur un frottis cervical, à condition que celui-ci soit placé dans un milieu de transport adapté, respectant l’intégrité du génome viral. Il en existe deux types : milieux spécifiques (ex. Specimen Transport Medium, Digne) ou milieux destinés à la cytologie en milieu liquide, agréés pour la biologie moléculaire (seuls deux sont validés : PreservCyt® de Cytyc et SurePath® de TriPath). Le génotypage peut également être réalisé sur un prélèvement tissulaire (biopsie ou pièce opératoire). Les tissus frais sont préférables aux tissus fixés et inclus en paraffine. Les techniques de génotypage actuelles comprennent typiquement trois étapes : extraction d’ADN ; amplification par PCR multiplexe à large spectre ; révélation des produits d’amplification par hybridation inverse, puces à ADN, technique Luminex ou encore pyroséquençage. Différents systèmes d’amorces àlarge spectre existent, ciblant majoritairement la région L1 du génome des HPV. Les systèmes de PCR HPV doivent répondre à un certain nombre de contraintes : le risque de réactions croisées dues à la diversité des génotypes HPV, la compétition entre les cibles due à la fréquence des infections multiples, le risque de faux négatifs dus à des délétions de fragments du génome viral lors de son intégration au génome de la cellule hôte, un seuil de sensibilité adapté à l’application visée. L’utilisation de la PCR, dans le contexte du génotypage, nécessite une validation rigoureuse et des contrôles adéquats, en particulier en ce qui concerne le système d’amorces à large spectre utilisé. Les seuils de sensibilité sont variables en fonction des génotypes amplifiés. Les différentes techniques disponibles utilisent des systèmes d’amorces différents, et les spectres d’HPV mis en évidence sont variables (tableau). Spectre des HPV détectés par différentes méthodes de génotypage. Désignation du système de génotypage (fabricant ou référence) HPV à haut risque HPV probablement à haut risque HPV à bas risque HPV à risque indéterminé Inno-Lipa (Inno Genetics) 16, 18, 31, 33, 35, 39, 45,51, 52, 56, 58, 59, 68 53,66 6, 11, 40, 42, 43, 44, 54, 70 74 Linear Array (Roche Diagnostics) 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68,73, 82 26,53,66 6, 11, 40, 42, 54,61, 70, 72, 81,CP6108 55, 62, 64, 67, 69, 71, 83, 84, IS39 Papillo check (Greiner bioOne) 16, 18, 31, 33, 35, 39,45, 51, 52, 56, 58, 59, 68, 73, 82 53,66 6, 11, 40, 42, 43, 44, 70 Clinical Array HPV (Genomica) 16, 18, 31, 33, 35, 39,45, 51, 52, 56, 58, 59, 68, 73, 82 26,53,66 6, 11, 40, 42, 43, 44, 54, 61, 70, 72,81, 89 62, 71, 83, 84, 85 Multiplex Human Papillomavirus Genotyping (Schmitt 2006) 16, 18, 31, 33, 35, 39,45, 51, 52, 56, 58, 59, 68, 73, 82 66 6, 11, 42, 43, 44,70 * Les 13 HPV à haut risque les plus courants apparaissent en gras En tout état de cause, le spectre des HPV proposé par ces différentes techniques est plus adapté à l’utilisation en recherche qu’en clinique, puisqu’il comprend de nombreux HPV à bas risque et à risque inconnu. Par ailleurs, la multiplication des techniques disponibles et les inévitables discordances intratechniques appelle à la prudence et nécessiterait une standardisation. Préalables à l’utilisation du génotypage en pratique clinique Dans le domaine de la recherche, l’intérêt du génotypage est évident, tant pour estimer les prévalences spécifiques de types dans une population donnée, que pour évaluer l’importance des infections simples et multiples, pour attester d’une persistance spécifique de type, estimer un risque spécifique de type de progression vers une lésion intra-épithéliale de haut grade du col utérin, ou pour surveiller les cohortes de femmes vaccinées avec les vaccins prophylactiques ou thérapeutiques, etc. En pratique clinique, l’intérêt de la détection des HPV en agrégat de 13 HPV à haut risque a été largement démontré, en particulier dans le tri des frottis ASC-US, dans la surveillance post-traitement des lésions de haut grade, et en dépistage primaire. Les progrès techniques, qui rendent aujourd’hui la réalisation du génotypage à large échelle possible, posent la question de la place de l’utilisation du génotypage en pratique clinique : le génotypage HPV pourrait-il améliorer le dépistage, la surveillance et la prise en charge des lésions précancéreuses du col utérin ? On attend en particulier une amélioration en termes de spécificité du test HPV. L’objectif d’un biomarqueur additionnel au test HPV classique serait de fournir une stratification en fonction du risque de lésion précancéreuse du col, afin d’adapter la prise en charge : attitude moins agressive en cas de risque moins élevé et, au contraire attitude plus agressive en cas de risque augmenté. Dans ce contexte, il convient tout d’abord de définir sous quelle forme ce génotypage doit être réalisé. Choix des génotypes HPV utiles à identifier pour les applications cliniques Ce choix doit se faire sur des critères objectifs que sont une valeur prédictive positive élevée, une fraction attribuable élevée et une probabilité d’évolution vers un cancer élevée. Les HPV 16 et 18 répondent clairement à ces différents critères quelle que soit la région géographique envisagée. L’importance des autres types HPV, en revanche, est variable en fonction de la région géographique. En tout état de cause, seuls les HPV à haut risque et potentiellement à haut risque paraissent intéressants à génotyper en pratique clinique. Résultats à considérer Le génotypage peut conduire à deux types de résultats intéressants en clinique : soit la simple identification de la présence d’un HPV plus agressif (comme l’HPV 16) à un temps « t », soit l’identification répétée d’un même type oncogène (persistance d’un type) sur plusieurs prélèvements successifs. C’est cette persistance qui renferme la notion de risque la plus importante. Format des tests de génotypage Il peut être envisagé de faire soit successivement un test HPV-HR en agrégat, puis un génotypage, soit d’emblée un génotypage qui viendrait remplacer le test HPV en agrégat. Cette seconde possibilité ne devient possible, bien entendu, que si les coûts du génotypage sont quasi équivalents au coût du test en agrégat, ce qui semble envisageable aujourd’hui avec les systèmes de puces. Pour chacune de ces solutions, on peut envisager soit un génotypage partiel (HPV 16 et 18, ± quelques autres ?) soit un génotypage complet de tous les types HPV à haut risque. Contextes potentiels d’utilisation du génotypage en pratique clinique Dans un contexte de dépistage primaire, les femmes présentant un frottis normal et un test HPV-HR en agrégat positif pourraient bénéficier d’un génotypage : les patientes positives pour HPV16 et/ou 18 pourraient être référées directement en colposcopie, les patientes positives pour d’autres types que les HPV 16 et 18 pourraient être contrôlées à 1 an. Le génotypage pourrait également avoir un intérêt en suivi postconisation, avec toujours un risque accru associé aux HPV 16 et 18. Le génotypage pourrait également être utilisé pour le suivi des patientes ayant plusieurs tests HPV-HR en agrégat positifs, pour identifier s’il s’agit d’une infection persistante à un type donné (risque majoré) ou des infections successives avec des types différents (risque moindre). Enfin, le génotypage pourrait également être utilisé comme critère d’éligibilité des femmes sexuellement actives à une vaccination prophylactique. Dans tous les cas, l’utilisation du génotypage en pratique clinique dépendra étroitement du format de génotypage envisagé : génotypage d’emblée ou suite à un test HPV-HR en agrégat positif. Points à retenir Les HPV 16 et 18 sont associés à un risque majoré de développer une lésion (pré)cancéreuse du col utérin. Plusieurs techniques de génotypage sont disponibles, mais restent chères et sont des tests qui ont été conçus dans une optique de recherche. Les techniques de génotypage doivent être rigoureusement validées et nécessiteraient une standardisation. Il est important de définir le format de génotypage le plus efficace pour des objectifs cliniques. Il est indispensable d’évaluer les performances cliniques du génotypage avant de l’intégrer aux algorithmes de prise en charge des lésions du col utérin. En pratique Avant de recommander l’utilisation du génotypage en clinique et de l’intégrer à des algorithmes de dépistage et de suivi des lésions précancéreuses du col utérin, il paraît aujourd’hui indispensable de définir quel format de génotypage sera le plus efficace pour des objectifs cliniques et d’évaluer la performance clinique de ces tests de génotypage en termes de sensibilité et de valeur prédictive positive. L’utilité potentielle du génotypage doit être également pesée en termes de coût, de faisabilité pour les laboratoires, de complexité d’interprétation des résultats pour les cliniciens. Cependant, il est clair que l’identification des HPV 16 et 18 est d’ores et déjà un marqueur de risque majoré, et incite donc à proposer une prise en charge particulièrement vigilante aux patientes qui en sont porteuses.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :






