Chirurgie
Publié le 28 fév 2025Lecture 11 min
La cure d’isthmocèle : hystéroscopique ou cœlioscopique ?
Laura MIQUEL, Aubert AGOSTINI, Pôle femmes‐parents‐enfants, hôpital de la Conception, AP‐HM, Marseille
La césarienne concerne 21,4 % des naissances en France selon l’enquête nationale périnatale de 2021, soit environ 150 000 procédures par an(1). L’isthmocèle reste encore peu étudié et sa prise en charge demeure insuffisamment codifiée. Bien qu’il ait été décrit pour la première fois en 1961, il a suscité moins de recherches par rapport à d’autres pathologies comme le placenta prævia, et reste relativement méconnu des praticiens(2). Pourtant, l’isthmocèle est lié à des symptômes parfois très invalidants dont la prise en charge adaptée peut améliorer la qualité de vie des femmes.
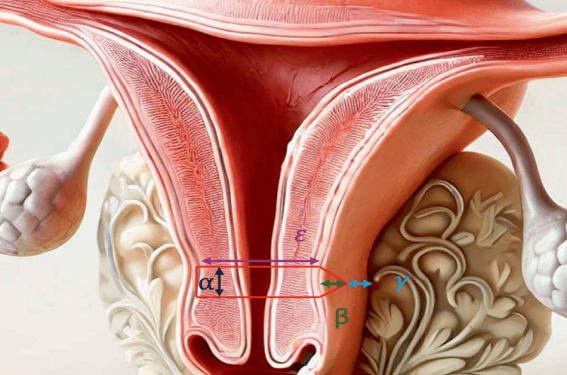
L'isthmocèle désigne une anomalie de cicatrisation survenant au niveau de l’hystérotomie après une césarienne. Elle se manifeste par une hernie de la cavité utérine qui s’enfonce dans l’isthme utérin. Les définitions de l’isthmocèle varient considérablement dans la littérature, selon les auteurs, et s’appuient principalement sur des seuils de mesure de la profondeur de l’encoche cicatricielle observée à l’échographie ou par hystéro‐sonographie. En réponse à cette diversité de définitions, Jordans et coll. ont établi un consensus d’experts selon la méthode Delphi(3). Il en ressort que l’isthmocèle est caractérisé en échographie par une encoche de plus de 2 mm dans le myomètre, observée sur une coupe sagittale médiane. En plus de la profondeur (β), ce consensus recommande de documenter d’autres paramètres échographiques comme la longueur de l’encoche (α), l’épaisseur du myomètre résiduel (·) ainsi que la largeur de l’encoche sur une coupe transversale (ε) (figure 1).
Figure 1. Coupe 3D de l’utérus représentant un isthmocèle et les mesures de celui‐ci selon Jordans et coll.(3).
L’estimation de la prévalence de l’isthmocèle est complexe en raison de la variété des définitions, des méthodes diagnostiques utilisées (échographie, hystérosonographie, hystéroscopie, IRM), du moment de l’examen et du type de population étudiée (symptomatique, infertile, ou recherchée de manière systématique). Cette encoche cicatricielle post‐césarienne est fréquemment observée, y compris chez des femmes sans symptômes ni facteurs de risque particuliers. En prenant comme critère principal l’encoche de plus de 2 mm, l’isthmocèle a été observée par échographie dans 45,6 à 49,6 % des cas chez des patientes présentant un utérus cicatriciel, et dans 64,5 % des cas par hystérosonographie(4,5). Cependant, ce critère, purement fondé sur l’imagerie, ne semble pas suffisamment discriminant pour différencier l’isthmocèle, considéré comme une pathologie potentiellement induite par la césarienne, d’une variation normale de la cicatrisation.
Symptômes
Le « syndrome de la cicatrice de césarienne » se définit habituellement par l’association d’un isthmocèle visible à l’échographie et de troubles menstruels : allongement des cycles, spottings à J10 caractéristiques, saignements post‐coïtaux, et/ou des douleurs pelviennes(6‐10). Les spottings menstruels entraînent une altération marquée de la qualité de vie des femmes avec une détérioration de l’estime de soi, de l’efficience professionnelle, de la qualité de la vie sexuelle et des activités de loisir. Plusieurs études prospectives menées auprès de femmes ayant subi une césarienne ont démontré que ces symptômes étaient significativement plus fréquents en présence d’un isthmocèle, surtout si celui‐ci est de grande taille. Les douleurs pelviennes tendent à être plus fréquentes lorsque le pourcentage du myomètre résiduel est inférieur à 25 %(10). Les spottings, les dysménorrhées ainsi que les douleurs pelviennes chroniques augmentent également avec la longueur et la largeur de l’isthmocèle(6,8). De plus, les spottings semblent particulièrement corrélés à une indentation cicatricielle plus profonde ou à un volume important de l’isthmocèle, tel que mesuré par reconstruction en 3D(11).
Enfin, les complications obstétricales ne sont pas à négliger avec les grossesses sur cicatrice de césarienne, les placenta accreta, increta, percreta et enfin les ruptures utérines. Cependant l’existence ou non d’un isthmocèle ou d’un « syndrome de la cicatrice de césarienne » n’est pas retrouvé en soi dans la littérature comme un facteur de risque supplémentaire de ces complications propres à l’utérus cicatriciel.
Cure hystéroscopique
Le traitement chirurgical de correction par voie hystéroscopique est couramment utilisé pour les isthmocèles présentant une épaisseur suffisante du myomètre résiduel. Cette épaisseur minimale varie selon les auteurs de > 2 mm à > 2,5 mm, bien que ces seuils ne soient pas fondés sur des études comparatives. Certains spécialistes déconseillent cette approche en cas de désir de grossesse, tandis que d’autres augmentent le seuil du myomètre résiduel à > 3,5 mm pour justifier l’utilisation de l’hystéroscopie dans ces cas(12,13).
Le traitement hystéroscopique se déroule généralement selon le protocole suivant :
– résection de la berge inférieure de l’isthmocèle à l’aide d’une anse diathermique en section pure (figure 2) ;
– parfois, la berge supérieure de l’isthmocèle est également réséquée, bien que cette approche n’ait pas démontré de supériorité ;
– fulguration, électrocoagulation au rollerball, ou résection du fond de l’isthmocèle(12) (figure 3).
Figure 2. Résection de la berge inférieure de l’isthmocèle à l’aide d’une anse diathermique en section pure.
Figure 3. Fulguration, électrocoagulation au rollerball ou résection du fond de l’isthmocèle.
Dans leur étude randomisée de 2018 comparant la chirurgie à une gestion expectative, Vervoort et coll. ont prouvé l’efficacité de ce traitement pour les spottings liés à l’isthmocèle(14). En analysant 18 études, Al Mutairi et coll. ont conclu à une amélioration des symptômes (saignements et douleurs) dans 92,8 % des cas(15). Mashiach et coll., dans une revue de 21 articles, ont rapporté une amélioration des saignements dans 60 à 100 % des cas(16). Vitale et coll., après avoir examiné 15 études, ont constaté une amélioration des saignements dans 85 % des cas(17). Cependant, certains facteurs peuvent influencer les résultats, notamment la rétroversion de l’utérus, un myomètre résiduel fin, des isthmocèles situés en hauteur et des césariennes multiples(18,19). Après l’opération, l’épaisseur du muscle résiduel varie entre 4,2 et 5,7 mm, ce qui est inférieur aux autres techniques(12). Peu de complications ont été observées, avec un taux de 0,76 % selon la méta‐analyse de Vitale et coll(17). Vervoort et coll. ont rapporté 2 % de cas d’infections pelviennes(14).
Pour les femmes avec un désir de grossesse, dans la méta‐analyse de Al Mutairi et coll., 18 études ont été évaluées et ont rapporté un taux de grossesse de 69,8 %(15). Un utérus rétroversé peut constituer un facteur de mauvais pronostic pour la conception, tandis qu’une augmentation de l’épaisseur du myomètre après l’intervention est associée à un meilleur pronostic de grossesse(20,21). Lors d’une prise en charge en AMP, cette technique peu invasive peut se révéler particulièrement inté ressante en cas de transfert difficile, voire impossible lors d’un isthmocèle volumineux (figure 4).
Figure 4. A : coupe IRM sagittale de l’utérus. Volumineuse isthmocèle rendant le transfert embryonnaire impossible. B : coupe IRM sagittale de l’utérus après résection hystéroscopique. Transfert embryonnaire possible.
Cure cœlioscopique
La voie cœlioscopique est généralement réservée aux cas où le traitement hystéroscopique est contre‐indiqué, notamment pour les isthmocèles avec un myomètre résiduel fin. La procédure chirurgicale classique inclut les étapes suivantes(22) :
– adhésiolyse vésico‐utérine (figure 5A) ;
– dissection de la vessie (figure 5B) ;
– ouverture de l’isthmocèle (figure 5C) ;
– excision complète des bords de l’isthmocèle jusqu’au canal cervical, avec l’insertion d’une bougie dans ce dernier (figure 5D) ;
– suture en un ou deux plans de la néo‐hystérotomie (figure 5E) ;
– +/‐ Traitement de la rétroflexion utérine si nécessaire.
Certains auteurs ont suggéré de faciliter le repérage de l’isthmocèle pendant la cœlioscopie en utilisant la transillumination via une hystéroscopie réalisée simultanément, une technique appelée « Halloween sign » (figure 5F)(23). Il est également recommandé d’effectuer un test de perméabilité tubaire avant l’incision. Cette procédure peut aussi être réalisée en chirurgie robotique(24).
5A. Adhésiolyse vésico‐utérine.
5B. Dissection de la vessie.
5C. Ouverture de l’isthmocèle.
5D. Excision complète des bords de l’isthmocèle jusqu’au canal cervical, avec l’insertion d’une bougie dans ce dernier.
5E. Suture en un ou deux plans de la néo‐hystérotomie.
5F. Technique de transillumination de l’isthmocèle via hystéroscopie réalisée simultanément (« Halloween sign »).
Figure 5. Procédure chirurgicale par voie cœlioscopique.
La revue systématique de Mashiach et coll. a montré une amélioration des saignements dans 78 à 94 % des cas(16). Vitale et coll. ont re trouvé une amélioration dans 92,8 % des cas(17). Après l’opération, l’épaisseur du muscle résiduel est en moyenne de 10 mm(12). Les récidives d’isthmocèles varient entre 1,6 et 33 %, tandis que peu de complications ont été rapportées, avec un taux de 1,7 %(17). Vervoort et coll. ont noté 2 % de cas de plaies vésicales, et Delaine et coll. ont rapporté une hémorragie génitale à J10 ayant nécessité une transfusion sanguine(22,25).
Pour les patientes cherchant à concevoir, les taux de grossesse après cette intervention varient de 37,5 à 90 %(16).
Cure vaginale
Cette voie chirurgicale, bien que moins étudiée, partage les mêmes indications que la voie cœlioscopique. Le déroulement de l’intervention suit généralement les étapes suivantes(26) :
– infiltration vagin ;
– dissection de la vessie ;
– ouverture de l’isthmocèle ;
– excision complète des bords de l’isthmocèle jusqu’au canal cervical ;
– suture en un ou deux plans de la néo‐hystérotomie.
Dans leur méta‐analyse, Vitale et coll. ont rapporté une amélioration des saignements dans 82,5 % des cas(17). Après l’opération, l’épaisseur du muscle résiduel varie entre 5,6 et 8,95 mm. Les complications sont rares, avec un taux de 2,2 %. Les principales complications incluent des hématomes (2,5 %), des infections pelviennes (2,4 %) et des plaies vésicales (2 %). Pour les femmes souhaitant concevoir, des grossesses intra‐utérines ont été observées dans 39,2 à 70,2 % des cas, avec 2,3 % de grossesses sur cicatrice(26,27).
Isthmocèle et infertilité
L’association entre isthmocèle et infertilité a longtemps été suspectée mais peu d’études venait corroborer cette hypothèse. Les antécédents de césarienne pourraient réduire les chances de naissance vivante, que ce soit de manière naturelle ou après un recours à l’AMP(28). Cependant, le rôle spécifique de l’isthmocèle dans l’infertilité reste à ce jour incertain.
Les données concernant l’impact de l’isthmocèle sur la fertilité spontanée sont limitées. Une étude rétrospective portant sur 35 patientes présentant un isthmocèle symptomatique a mis en évidence une infertilité plus fréquente chez les femmes ayant un isthmocèle plus sévère (selon le score de Tower)(29). Cette même étude a rapporté un taux de grossesse de 44 % après traitement de l’isthmocèle. Selon la dernière méta‐analyse de Vitagliano et coll., chez les femmes en cours de FIV, le taux de naissance vivante après transfert d’embryon est plus faible chez les femmes présentant un isthmocèle que chez celles ayant déjà subi une césarienne sans isthmocèle (OR : 0,56 ; IC 95%, 0,49‐0,65 ; I2 = 0 ; p < 0,00001 ; RD, − 0,12 ; IC 95%, − 0,15 à − 0,09)(30). Dans leur étude de cohorte de 2023, Mensi et coll. ont étudié 114 femmes présentant un antécédent d’accouchement par césarienne et une indication de FIV(31). Soixante‐seize femmes ont été diagnostiquées avec un isthmocèle, soit 67 % (IC 95 % : 58 à 75 %). Les caractéristiques de base des femmes avec et sans isthmocèle étaient similaires. En revanche, le taux de grossesse clinique (OR ajusté 0,31 ; IC 95 % : 0,13 à 0,72) et le taux de naissance vivante (OR ajusté 0,38 ; IC 95 % : 0,17 à 0,86) étaient significativement plus faibles chez les femmes affectées.
Quand opérer ?
S’il apparaît de plus en plus clair que l’isthmocèle est un facteur de mauvais pronostic pour l’obtention d’une grossesse chez la femme infertile, la correction chirurgicale de celle‐ci n’améliorerait pas forcément les taux de naissance vivante. Les études observationnelles non comparatives après chirurgie retrouvent des taux de grossesse entre 25 et 100 %(29). Lors de la mise à jour des RPC du CNGOF pour la prise en charge initiale du couple infertile, les experts ont conclu que, chez la femme infertile, il n’est probablement pas recommandé de réaliser une cure d’isthmocèle asymptomatique (pas de douleurs, pas de métrorragie, pas d’antécédent de grossesse sur cicatrice)(32). Concernant le traitement des isthmocèles symptomatiques, la revue systématique de la littérature de Harjee et coll. de 2021 avait retrouvé 13 études, dont un essai contrôlé randomisé, 6 séries de cas prospectifs et 6 séries de cas rétrospectifs décrivant 234 patients ayant subi une intervention chirurgicale pour une isthmocèle et une infertilité secondaire(33). Au total, 188 patientes avaient été traitées par hystéroscopie, 36 par laparoscopie, 7 par laparotomie et 3 par voie vaginale. Au total, 153 des 234 patientes (65,4 %) avaient obtenu une grossesse dans toutes les études au cours de leurs périodes d’étude respectives. Les taux de grossesse dans l’essai contrôlé randomisé étaient de 21 sur 28 (75 %) pour les patientes traitées par hystéroscopie, contre 9 sur 28 (32 %) pour les patientes non traitées. Parmi les études rapportant des résultats de grossesse, 101 des 116 (87,1 %) grossesses avaient abouti à une naissance vivante. L’incidence des événements indésirables était de 2 %, y compris le risque de réintervention. Les auteurs proposent un diagramme décisionnel tel que décrit dans l’algorithme.
Algorithme. Algorithme décisionnel de traitement selon Harjee et coll.(34).
En conclusion
L’isthmocèle se définit par une encoche > 2 mm dans le myomètre post‐césarienne, visible en échographie. Un diagnostic précis utilise plusieurs paramètres échographiques : longueur (α), profondeur (β), épaisseur du myomètre résiduel (·), et largeur (ε). La confirmation peut être faite par échographie, hystérosonographie ou IRM(3). Il est important de prendre en compte les symptômes associés(6‐10).
Le traitement est envisagé si l’isthmocèle est symptomatique (troubles menstruels, douleurs, infertilité). En l’absence de symptômes, la prise en charge n’est pas recommandée, surtout pour les femmes sans désir de grossesse(32).
L’hystéroscopie est la première option pour les isthmocèles avec myomètre résiduel > 2 mm, notamment pour améliorer les saignements et douleurs. Elle est évitée si désir de grossesse, sauf si le myomètre résiduel est > 3,5 mm. Elle montre une amélioration des symptômes dans 60 à 100 % des cas(12,13).
La cœlioscopie est préférée pour les isthmocèles complexes ou avec myomètre très fin. Elle permet une restauration complète de la paroi utérine, avec une réduction du taux de récidive. Elle améliore les symptômes dans 78 à 94 % des cas, avec une épaisseur myométriale postopératoire plus importante qu’après hystéroscopie, bénéfique pour les patientes avec désir de grossesse(16). La voie vaginale est une alternative dans certains cas, avec un bon taux de succès pour les saignements, mais elle est moins étudiée(26). Les risques sont limités : 0,76 % de complications pour l’hystéroscopie et environ 1,7 % pour la cœlioscopie(17).
Les femmes avec isthmocèle peuvent avoir un taux de grossesse réduit en FIV. La chirurgie améliore souvent les symptômes mais n’augmente pas systématiquement les taux de naissance vivante. En présence de symptômes à type de métrorragies post‐cataméniales, de douleurs pelviennes peu systématisées, d’infertilité secondaire mal expliquée, il peut sembler licite d’envisager le traitement d’un isthmocèle.
L’isthmocèle ne doit pas être une pathologie créée par l’imagerie, et l’abstention sera de rigueur en cas de découverte fortuite lors d’un examen.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :