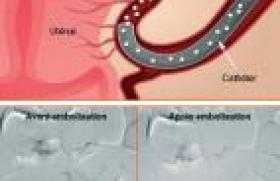
Utérus
Publié le 30 oct 2024Lecture 6 min
Transplantation utérine : d’immenses progrès malgré les difficultés
Denise CARO, d’après la communication du Pr Vincent Lavoué

La transplantation utérine constitue un nouvel espoir de grossesse chez les femmes qui souffrent d’infertilité utérine absolue, définie par l’absence d’utérus soit d’origine congénitale (principalement syndrome de Mayer-Rokitansky-Küster-Hauser) soit acquise (hystérectomie pour hémostase ou cancer). C’est l’ouverture d’un champ extraordinaire de recherche en chirurgie, en infertilité et en transplantation. C’est la première et la seule greffe éphémère de l’histoire, l’utérus étant retiré après avoir permis (ou pas) la naissance d’enfants vivants afin de ne pas prolonger le traitement immunosuppresseur au-delà de 6 ans.
Si la première tentative de transplantation utérine (TU) a eu lieu en 2000 en Arabie Saoudite, c’est en 2014 en Suède que la première greffe d’utérus a permis de donner naissance à un enfant vivant. On estime aujourd’hui que 150 transplantations utérines ont été réalisées dans le monde donnant naissance à 75 enfants. Dès le début des TU, deux approches très différentes se sont développées : les transplantations avec donneuses en état de mort encéphalique (EME) et celles avec donneuses vivantes.
En France, depuis 2019, trois TU ont été réalisées à partir de donneuses vivantes dans le service du Pr Jean‐Marc Ayoubi à l’hôpital Foch (Suresnes) : une s’est soldée par un échec, une autre par la naissance d’un enfant vivant et la troisième a permis de mener à bien deux grossesses.
Dès 2015, le Pr Tristan Gauthier au CHU de Limoges a tenté des TU avec des donneuses en EME ; le projet a été arrêté en 2018 sans naissance d’enfant vivant. À l’initiative du Pr Vincent Lavoué, le programme TULIpE (Transplantation Uterus with Living and dEceases donors) vient de commencer au CHU de Rennes.
Un parcours long et complexe
Après que l’indication de TU chez une femme atteinte de fertilité utérine définitive est posée, le chemin menant à une éventuelle grossesse est long, complexe et semé d’embûches.
La première étape consiste à obtenir, par fécondation in vitro (FIV), six embryons au stade J5 congelés (nécessitant plusieurs cycles d’induction d’ovulation et de FIV). Sans cette réserve, la TU n’est pas envisagée.
Il s’agit ensuite de rechercher une donneuse vivante compatible et/ou un organe issu d’une donneuse en EME (la patiente est alors inscrite sur la liste nationale des personnes en attente de greffon). La possibilité de trouver une donneuse vivante compatible (famille ou amie) est limitée, et l’attente d’un organe issu d’une personne en EME peut durer plusieurs années.
Si cette étape importante est franchie, la patiente n’est pas encore arrivée au bout de ce parcours du combattant. Après la transplantation, il faut attendre un an pour savoir s’il y aura ou non un rejet (qui arrive dans 60 à 70 % des cas) et pour vérifier l’absence d’infection opportuniste due au traitement immunosuppresseur.
Si, après 9 mois, la greffe est stable, le tacrolimus contre‐indiqué pendant la grossesse est remplacé par l’azathioprine. Et c’est enfin, et seulement après avoir à nouveau vérifié que la greffe reste stable à la suite de ce changement, que l’on autorise le transfert d’embryons. La grossesse – si elle n’est pas interrompue – se solde forcément par une césarienne programmée à 37 semaines d’aménorrhée (SA), sachant que les naissances ont lieu à 35 SA en moyenne. Après une grossesse réussie, on peut proposer à la patiente d’en tenter une seconde. Dans tous les cas, on explante l’utérus greffé dans les 6 ans pour arrêter les immuno‐ suppresseurs et éviter les complications liées à ce traitement(1).
Avantages et inconvénients de chaque type de don
Outre la question de l’accès à un greffon compatible, quels sont les chances de succès et les risques encourus avec l’un et l’autre type de don ?
En termes de succès de la greffe, un avantage (modeste) revient au don à partir d’une personne vivante. En effet, dans ce cas, il est possible d’étudier précisément la qualité de l’utérus (IRM, hystéroscopie) à prélever. À noter que la donneuse potentielle doit avoir entre 38‐40 ans et 63 ans et avoir réalisé son projet de parentalité. L’organisation du prélèvement et de la transplantation est plus facile qu’avec une donneuse en EME. En revanche, l’intervention pour prélever l’utérus est longue (entre 6 et 11 heures selon les techniques) et non dénuée de risques (hémorragie, infections, fistules vésico‐vaginales, insuffisance ovarienne, mortalité < 1/100 000). Toutefois, les techniques tendent à se simplifier avec une meilleure connaissance de la vascularisation utérine, de ses variations(2) et grâce à l’apport des robots(3).
À l’inverse, la qualité du greffon issu d’une donneuse en EME ne peut être évaluée que succinctement, et il n’y a pas d’interdiction à prélever chez une femme plus jeune. Techniquement, il est possible d’obtenir un utérus avec un arbre vasculaire plus long, ce qui offre la possibilité de faire la greffe sur les vaisseaux iliaques externes.
Une autre difficulté est de parvenir à prélever un utérus sans compromettre le prélèvement d’autres organes (vitaux).
Avant l’intervention des autres équipes de prélèvement, on procède à une dissection du triangle de Scarpa pour faire une canalisation artérielle bilatérale et une décharge veineuse unilatérale fémorale. On contourne tous les systèmes artériels et veineux et on canule l’artère sans exsanguiner la patiente, ce qui compromettrait le prélèvement des autres organes. On laisse les autres équipes canuler en aortique et en cave, et on rem place la masse sanguine par le produit de conservation. L’utérus est prélevé en dernier, car ce n’est pas un organe vital et qu’il y a un risque de contamination des organes vitaux par la filière génitale. Dans tous les cas, après le prélèvement, il y a de longues heures de préparation du greffon.
En dépit des difficultés les efforts se poursuivent
Un des principaux freins à la TU réside dans la difficulté à obtenir un greffon donneuse/receveuse compatible. La possibilité d’avoir une personne de sa famille compatible prête à donner son utérus est assez faible, le besoin de greffons à partir de femmes décédées est donc important. Or, selon la base Cristal, 126 greffons potentiels ont été prélevés en 6 ans (entre 2014 et 2019), soit un peu plus d’une vingtaine par an en France, sans compter les refus des familles, les difficultés logistiques (éloignement entre donneuse et receveuse) et les problèmes de compatibilité groupe ABO, ce qui est très peu(4). Cependant, en dépit des diffi‐cultés et de la lourdeur de l’orga nisation, les TU se poursuivent.
Pour preuve, le programme TULIpE initié par le CHU de Rennes, qui a obtenu son financement de la part du Programme hospitalier de recherche clinique (PHRC) en juin 2021, un accord de l’Agence nationale de sécurité du médicament et des produits de santé (ANSM) en mai 2023 et qui a débuté officiellement fin décembre 2023. Il inclura huit couples donneuses vivantes/receveuses et huit autres donneuses en EME/receveuses.
« Les deux approches sont complémentaires, a estimé le Pr Vincent Lavoué, l’avenir dira si l’une prend le pas sur l’autre. La greffe d’utérus pose également la question de sa place par rapport à la gestation pour autrui interdite en France mais à laquelle certaines patientes ont recours à l’étranger. Il n’est pas exceptionnel qu’une femme fasse les deux démarches en parallèle sans savoir laquelle portera ses fruits en premier. »
D’après la communication du Pr Vincent Lavoué (CHU de Rennes), 21es journées de chirurgie gynécologique et pelvienne (SCGP), septembre 2024.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :