Cancérologie
Publié le 15 aoû 2011Lecture 8 min
Néoplasies intraépithéliales de la vulve
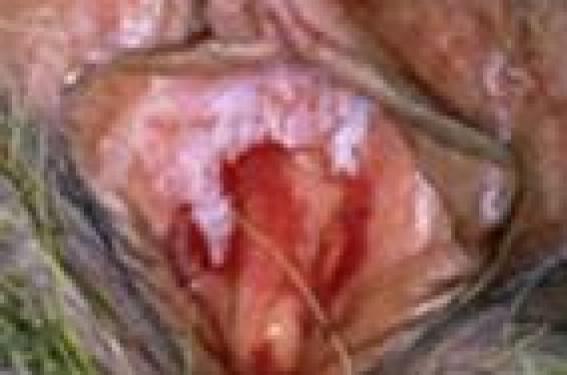
Le terme de néoplasie intraépithéliale de la vulve (vulvar intra-epithelial neoplasia, VIN) définit les néoplasies intra-épithéliales précarcinomateuses, développées à partir des kératinocytes. Ainsi, la maladie de Paget et les proliférations mélanocytaires en sont exclues. Le terme de VIN ne correspond pas à une entité isolée. Il recouvre plusieurs entités cliniques et anatomopathologiques différentes et tend à remplacer les appellations plus anciennes de maladie de Bowen, érythroplasie de Queyrat, papulose bowenoïde, dysplasies, atypies ou carcinome in situ.
Classification
À l’origine, la classification des VIN a été calquée sur celle des néoplasies cervicales (CIN). Un VIN est défini et caractérisé sur des critères purement histologiques : désorganisation et perte de l’architecture de l’épithélium avec atypies cellulaires, hyperchromasie, pléiomorphisme (anisocytose et anisocaryose), mitoses anormales et cellules monstrueuses. Si les anomalies cellulaires et architecturales se limitaient au tiers inférieur de l’épithélium, on parlait de VIN1, à sa moitié inférieure de VIN2 ou sur toute sa hauteur de VIN3. En fait, ces termes de VIN1, VIN2 et VIN3 ont été abandonnés au profit de VIN, car il n’y a pas de passage de VIN1 à VIN2, puis VIN3. Les VIN2 et VIN3 actuellement appelés VIN tout court sont des lésions de « haut grade » comportant un risque invasif, contrairement au VIN1 qui n’est pas un précurseur du cancer invasif. Aux VIN correspondent deux types de lésions bien différentes dans leur morphologie, leur histologie, leur biologie et leurs aspects cliniques que sont les usual VIN (UVIN), ou VIN classiques, et les differentiated VIN, ou VIN différenciés. Les UVIN, anciens VIN indifférenciés sont associés à des papillomavirus humains (HPV) oncogènes, alors que les VIN différenciés ne sont pas viro-induits, mais surviennent dans l’immense majorité des cas sur une dermatose préexistante (lichen scléreux voire lichen plan ou radiodermite).
VIN classiques ou UVIN
Aspects anatomopathologiques
L’aspect est ici celui d’un carcinome in situ peu différencié : l’épithélium est basophile avec une architecture désorganisée ; il existe des atypies sévères étagées sur toute la hauteur de l’épithélium et l’on note fréquemment la présence de koïlocytes, témoins d’une infection à HPV dans la couche granuleuse. L’atteinte des annexes est également possible. Certains auteurs subdivisent ces UVIN en deux groupes : VIN basaloïdes et VIN condylomateux. Ces images histologiques renvoient à des cliniques variées et surtout des pronostics bien différents ; c’est pourquoi, contrairement aux Anglo-Saxons, nous préférons garder les termes cliniques de maladie de Bowen, de papulose bowenoïde, et même isoler une variante à type de VIN confluent.
Étiopathogénie
Depuis ces dernières décennies, la fréquence des UVIN ne cesse de croître. Ils touchent souvent des femmes jeunes et certaines formes peuvent évoluer vers un cancer invasif vulvaire mais parfois aussi vers un cancer invasif anal. Comme les CIN, les UVIN sont associés, dans la majorité des cas, à une infection à HPV dits oncogènes (excluant donc les HPV 6 et 11) ; les HPV en cause sont le plus fréquemment HPV 16 et HPV 18, mais aussi HPV 31, 33, 39. Si cette notion est intéressante sur le plan carcinologique, elle ne présente aucun intérêt dans la pratique clinique, car il n’y a pas de parallélisme entre le type de virus, l’aspect clinique et le potentiel invasif ou non de la (ou les) lésion(s) ; il faut éviter de faire ces recherches virologiques inutiles et onéreuses. En revanche, chez ces femmes porteuses d’HPV oncogènes, il faut rechercher d’autres localisations du virus, en particulier au niveau du col, voire du vagin ou de l’anus. Dans les autres cofacteurs, on retrouve, comme les CIN, le tabagisme et parfois des déficits immunitaires. À une image histologique monomorphe de dysplasie sévère étagée sur toute la hauteur de l’épithélium, correspondent des aspects cliniques et évolutifs très différents : la maladie de Bowen, la papulose bowenoïde et le VIN confluent.
Figure 1. Maladie de Bowen.
• Maladie de Bowen (figure 1)
Individualisée en 1921 par Jessner (Bowen décrivit en 1912 l’affection cutanée qui porte son nom), la maladie de Bowen vulvaire touche le plus souvent la femme ménopausée. Elle est parfois prurigineuse ou cause de sensation de cuisson ou de brûlures, mais elle peut rester asymptomatique, découverte lors d’un examen gynécologique systématique. La lésion est uni- ou paucifocale, muqueuse et/ou cutanée, en plaques.
Cette ou ces plaques sont bien limitées en périphérie, polycycliques, rouges (forme érythroplasique), blanches (forme leucoplasique), érythroleucoplasiques et/ou pigmentées, légèrement en relief. L’aspect rouge est celui d’une érythroplasie vulvaire, équivalente de l’érythroplasie de Queyrat décrite chez l’homme. Elle pose le problème diagnostique d’une lésion érythroplasique vulvaire comme le lichen plan, le lichen scléreux ou une vulvite inflammatoire, et l’examen anatomopathologique en permet la distinction. Les formes leucoplasiques et érythroleucoplasiques posent un problème diagnostique avec un lichen scléreux ou une maladie de Paget. L’évolution se fait vers l’extension en surface mais avec aussi parfois, dans 5 à 20 % des cas, une extension au chorion avec une phase de micro-invasion, puis d’invasion franche.
On peut suspecter une évolution vers l’invasion devant l’existence d’une lésion bourgeonnante, d’une ulcération infiltrée ; mais parfois, cette invasion n’est détectée qu’à l’examen histologique. Le meilleur choix thérapeutique est donc l’exérèse chirurgicale simple de la ou des lésions. L’association avec un CIN n’est pas fréquente dans cette forme. Un suivi régulier s’impose pour dépister d’éventuelles récidives.
Figure 2. Papulose bowenoïde.
• la papulose bowenoïde (figure 2), individualisée en 1978 chez l’homme par Wade et Kopf pour décrire des lésions condylomateuses multiples des organes génitaux externes, d’évolution bénigne, pouvant même régresser spontanément, mais correspondant à une image histologique de carcinome in situ, elle s’observe aussi chez la femme jeune.
La papulose bowenoïde touche des femmes âgées de 20 à 40 ans et peut s’observer chez l’enfant. Elle est plurifocale, pouvant atteindre la région périvulvaire et/ou périanale et est souvent associée à des lésions dysplasiques du col ou à de banals condylomes génitaux.
La papulose est souvent asymptomatique ou responsable d’un prurit modéré ou d’une gêne lors des rapports. Les lésions sont mutifocales à type de papules planes pigmentées de quelques millimètres de diamètre ou de lésions pseudo-condylomateuses rosées, rouges ou violacées à surface lisse, squameuse ou verruqueuse. Les éléments peuvent être isolés les uns des autres ou confluer en placards papuleux avec une surface érythémateuse, parfois leucoplasique pigmentée ou polychrome. Le diagnostic se pose avec de simples condylomes, un lichen plan, des naevi ou des verrues séborrhéiques et la biopsie reste indispensable.
Du fait du caractère multicentrique de l’infection à HPV chez la femme jeune, un bilan complet s’impose : frottis cervicovaginaux, voire colposcopie, examen de la marge anale, voire du canal anal.
L’évolution est, dans l’extrême majorité des cas, parfaitement bénigne et comparable à celle des condymomes : persistance, guérison spontanée ou après traitement, récidives après traitement, quelle que soit la méthode utilisée. La destruction des lésions par applications d’imiquimod, de podophyllotoxine ou d’azote liquide, et la destruction par électrocoagulation ou au laser CO2 donnent de bons résultats cosmétiques.
Figure 4. VIN confluent invasif.
Figure 3. VIN confluent.
• VIn confluents (figures 3 et 4) Il n’en est pas de même des VIN dits « confluents » que nous tenons à isoler, qui surviennent souvent sur un terrain immunodéprimé et qui comportent un risque invasif important.
Les lésions sont chroniques et récidivantes après traitement. Elles sont prurigineuses, voire douloureuses et fissuraires. Elles réalisent des placards verrucoïdes, érythro-leucoplasiques plus ou moins pigmentés, à contours polylobés. Peu à peu, ils envahissent la muqueuse vulvaire et tendent à déborder en zone périnéale et périanale, voire à distance. L’existence de zones ulcérées, infiltrées ou indurées doit faire craindre une invasion et faire pratiquer des biopsies. Ces VIN confluents sont fréquemment associés à des lésions dysplasiques ou invasives du col ou de l’anus. Un état d’immunosuppression est souvent présent : maladie de Hodgkin, leucémie, lymphome, traitement immunosuppresseur pour maladie auto-immune ou transplantation d’organe, polyarthrite rhumatoïde, lupus, thrombopénie auto-immune.
Ces VIN s’observent plus fréquemment chez les femmes HIV+ ou porteuses du SIDA. Enfin, nous en avons observé plusieurs chez des femmes ayant un déficit idiopathique en CD4, d’où l’intérêt d’un dosage systématique des CD4 et des CD8. Il n’existe aucune tendance à la régression spontanée ; l’évolution est dominée par le risque d’apparition d’un ou plusieurs foyers de carcinome micro-invasif ou invasif non seulement au niveau de la vulve, mais aussi de l’anus. Le traitement est mal codifié, mais doit être chez ces femmes jeunes le moins mutilant ; le recours aux applications de 5-FU est souvent décevant, les applications d’imiquimod peuvent parfois faire partiellement régresser les lésions. La chirurgie conservatrice et les destructions au laser CO2 restent les traitements de choix. Quand il existe des zones suspectes, un ou plusieurs contrôles histologiques sont nécessaires. En cas de micro-invasion, inférieure à 1 mm, l’exérèse de la zone suffit, mais en cas d’invasion franche, la vulvectomie radicale doit être envisagée. Quels que soient les traitements, ces formes extensives justifient une surveillance très régulière, tri- ou quadri-annuelle.
VIN différenciés ou DVIN
Figure 5. VIN différencié.
Figure 6. VIN différencié.
Les anomalies cytologiques sont ici cantonnées à la couche basale ou dans le tiers inférieur de l’épithélium, il n’y a ici ni koïlocyte, ni HPV (figures 5 et 6).
Ces DVIN surviennent généralement sur une dermatose préexistante, le plus souvent un lichen scléreux, mais parfois un lichen plan leucoplasique ou érosif, voire une radiodermite. Ils font le lit du carcinome épidermoïde invasif de la vulve. Ils se développent surtout sur des lichens scléreux hyperplasiques non ou mal traités ; cette évolution est rare et ne survient que dans 3 à 6 % des lichens scléreux.
Il s’agit d’un cancer de la femme âgée qui représente 50 à 60 % des cancers invasifs vulvaires. En pratique, toute zone leucoplasique et/ou ulcérée, fixe, infiltrée et rebelle aux dermocorticoïdes puissants doit être biopsiée, car elle est suspecte de pouvoir correspondre à un DVIN.
L’évolution de ces DVIN se fait toujours vers le carcinome invasif, leur constatation impose une exérèse complète afin de rechercher des zones de micro-invasion, voire d’invasion franche.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :