Publié le 08 juin 2009Lecture 10 min
Comment prendre en charge une CIN 1
C. QUEREUX, J.-P. BORY, O. GRAESSLIN, Institut Mère-Enfant Alix de Champagne, CHU Reims
Autant la prise en charge d’une cytologie de haut grade est bien codifiée (colposcopie, biopsies et geste thérapeutique), autant celle d’un frottis de bas grade est beaucoup plus problématique car, lorsque l’on reçoit un tel frottis, il n’est pas du tout certain que la patiente présente une lésion méritant une prise en charge. Quand un CIN 1 est reconnu par l’histologie, la stratégie reste discutable entre l’abstention et un traitement destructeur
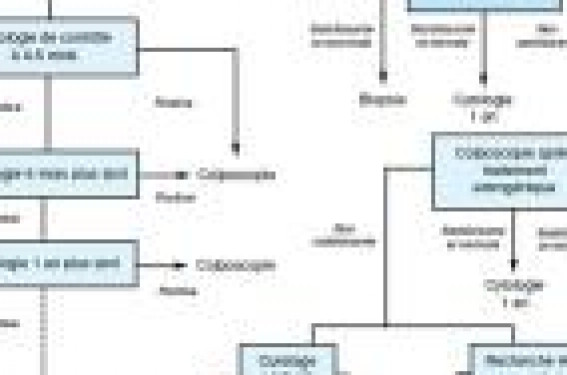
En 1988 à Bethesda, un comité d’experts du National Cancer Institute a proposé un nouveau rendu des résultats standardisés à l’échelon international, afin d’optimiser la prise en charge des patientes. Plusieurs actualisations ont eu lieu, dont la dernière en 2001. Les lésions virales (koïlocytes) sont regroupées avec les CIN 1 (dysplasies légères) dans la catégorie des lésions de bas grade. Au nombre d’environ 69 000 par an (en France sur un total de 6 millions, soit 1 à 2 %), les frottis de bas grade sont les anomalies cytologiques cervicales les plus fréquemment rencontrées après les ASC-US (2 à 4 %). Plaidoyer pour l’exploration Il est toujours problématique de prendre en charge les lésions de bas grade car, lorsqu’on reçoit un frottis de bas grade, il n’est pas du tout certain que la patiente présente un CIN de bas grade authentique. Il existe des diagnostics par excès mais aussi par défaut. Ainsi, une lésion de haut grade serait présente suite à un frottis de bas grade dans 15 à 30 % des cas, selon Solomon (1). Plusieurs stratégies sont possibles pour démasquer une lésion de haut grade derrière un frottis de bas grade. En France, dans ses recommandations de 2002, l’ANAES propose une alternative entre une colposcopie immédiate ou seulement en cas de frottis anormal ultérieur, réalisé tous les 6 mois, en revenant au dépistage classique après 3 frottis normaux successifs (figure). De notre point de vue, il est légitime de référer d’emblée ces patientes en colposcopie puisque près de 30 % de celles ayant un bas grade présumé, sont en réalité porteuses d’un haut grade au terme des investigations complètes. En pratique, le choix entre suivi cytologique ou colposcopie immédiate peut être influencé par l’âge de la patiente ; avant 25 ans, la moindre prévalence des hauts grades et la fréquente clairance spontanée des lésions de bas grade pourront faire préférer un suivi cytologique. La difficulté est réelle quand la zone de jonction n’est pas vue ; l’ANAES recommande alors deux stratégies possibles : – soit effectuer un curetage endocervical et, en cas de positivité, de compléter par une conisation diagnostique ; – soit effectuer un testing HPV et, en cas de positivité, de conseiller la conisation quand HPV+ et frottis+ sont reconfirmés. La valeur prédictive du test HPV semble supérieure au curetage de l’endocol. Ce test, quand il est négatif, permet de rassurer patiente et praticien, d’espacer les contrôles cytologiques à un an et d’éviter une conisation diagnostique. La recherche d’HPV oncogènes dans l’exploration d’un frottis de bas grade n’a pas d’intérêt du fait de la forte prévalence des HPV oncogènes dans les lésions de bas grade, 80 % dans l’étude ALTS (2). Dans la série de Pretorius (3), bien que le risque de développer un haut grade ultérieurement soit statistiquement plus élevé en cas de portage initial d’HPV oncogène (2,3 % vs 0,4 %), 78 % des patientes explorées étaient HPV+ à l’inclusion, chiffre proche des autres publications, ce qui limite l’intérêt de cette analyse dans cette indication. Arbre décisionnel devant un frottis de bas grade (recommandations 2002 de l’ANAES). Quels critères de traitement ? Une fois le diagnostic retenu, il y a débat sur la gestion des CIN de bas grade : surveillance ou traitement ? Cela dépend de l’histoire naturelle, de l’âge, de la persistance, de l’observance, etc. Sur quoi appuyer la décision ? L’évolution spontanée est souvent favorable et il faut en tenir compte. Ostor (4) en 1993 a publié une importante revue de la littérature portant sur l’histoire naturelle des dysplasies cervicales, où il montre que 56 % des CIN 1 vont régresser (30 % persistent, 10 % s’aggravent vers une dysplasie sévère, voire un cancer). Le taux de régression atteint même 90 % en 3 ans chez les plus jeunes, selon Moscicki (5) qui a suivi une population de jeunes femmes de 13 à 22 ans. Globalement, la régression est d’environ 50 % en moyenne entre 12 et 36 mois et il est légitime de cesser nos propos alarmistes et d’éviter de parler de précancer pour un bas grade qui n’est probablement pas la même maladie qu’un haut grade, même si tous les deux sont liés à l’action du virus HPV. Ce fort taux de régression spontanée est sans doute un élément rassurant qui pèse pour l’abstention thérapeutique. Le typage d’HPV Étant donné l’importante clairance spontanée des HPV oncogènes et des lésions de bas grade qui leur sont associées, la recherche d’HPV oncogène semble intéressante dans le suivi et peut s’avérer, en cas de persistance, un excellent indicateur de la logique d’un traitement. Walker (6), dans une série de 1 800 patientes présentant initialement une lésion de bas grade confirmée en colposcopie et histologie, a montré que le risque de développer un haut grade dans les 2 ans est significativement augmenté en cas de présence d’HPV lors de ce suivi (19 % vs 2 %, toutes cytologies confondues, 11 % vs 2 % si frottis normal, 19 % vs 3 % si frottis ASC-US ou bas grade). Dans le même sens, Guido (7) observe qu’une re-cherche d’HPV oncogène à 12 mois est plus performante que le frottis itératif : un test HPV seul à 12 mois est plus efficace que la cytologie itérative pour identifier le risque de développer un haut grade (92 vs 88 % pour une cytologie semestrielle). Cette stratégie semble d’autant plus intéressante chez les très jeunes femmes. Le coût est à la charge des patientes dans cette indication, ce qui en limite l’intérêt. L’avenir pourraît être dans le génotypage. Il est maintenant possible de déterminer la présence de certains HPV oncogènes particuliers de façon spécifique en routine (génotypage). Castle (8) s’est particulièrement intéressé au plus courant des HPV oncogènes : le type 16. Dans sa série de 5 000 patientes, il montre que, chez celles présentant un frottis de bas grade, la prévalence initiale de l’HPV 16 est de 21 %. Ces patientes auront un risque de développer un CIN 3 dans les 2 ans de 39 %, contre 10 % en présence d’un HPV oncogène autre que le 16 et 5 % en l’absence d’HPV oncogène courant. Il évoque ainsi la possibilité de traiter sans délai les patientes porteuses d’un bas grade HPV 16 à risque d’être perdues de vue. L’âge : critère décisionnel majeur Avant 30 ans, il existe des arguments : – pour la surveillance : en effet, le taux de régression spontanée est très élevé, traiter ne met pas à l’abri des récidives qui se produiront dans 6 à 10 % des cas, et il faut tenir compte du coût et de la complication des traitements. L’inconvénient est la possibilité des pertes de vue ; – pour le traitement : c’est normaliser une situation dont la pérennité entraîne un risque d’aggravation, une angoisse de la patiente, des problèmes relationnels, la multiplication des contrôles cyto-colpo-histologiques et le surcoût des suivis rapprochés. Après 45 ans, il faut être très méfiant car il y a souvent du haut grade associé au bas grade et fréquemment dans l’endocol : – si la colposcopie est satisfaisante, avec un trépied cyto-colpohistologique concordant, on peut se contenter d’un traitement par laser avec un contrôle dans les 3 à 6 mois ; – si la colposcopie n’est pas satisfaisante et a fortiori si le traitement n’est pas concordant, il est plus sage de conseiller une conisation. En pratique, trois critères majeurs sont en faveur du traitement : – un âge supérieur à 45-50 ans, – une pathologie persistante au-delà de 18 mois/2 ans, – et un risque élevé de perdu de vue et peut-être, dans l’avenir, un portage d’HPV type 16. Quel traitement ? Les traitements destructeurs Ces traitements (laser ++) ont la préférence à une double condition : – tout risque de gravité a été formellement éliminé, ce qui a pour corollaire que la colposcopie ne comporte aucun signe de « major change » ; – la lésion est observée dans sa totalité et donc la colposcopie doit être « satisfaisante ». Les traitements d’exérèse Avec contrôle histologique (ERAD, ECAD), les traitements d’exérèse sont recommandés dans les autres cas. Quelques conseils… Investiguez mais sachez ne pas déclencher la guerre des étoiles. Les frottis de bas grade doivent faire systématiquement rechercher une lésion de haut grade, masquée dans 15 à 30 % des cas. Longtemps, ce bilan a uniquement reposé sur la colposcopie, éventuellement précédée de frottis de contrôle. Le développement des techniques de recherche en routine de groupes d’HPV oncogènes permet de sélectionner lors du suivi ultérieur des patientes à risque augmenté de développer un haut grade. L’apparition de techniques de génotypage en routine, permettrait d’isoler dès le premier frottis de bas grade les patientes HPV 16 + qui sont à risque accru de lésion haut grade et pour lesquelles un traitement anticipé pourrait être choisi, limitant la probabilité d’être perdue de vue. Points à Retenir • Les frottis de bas grade doivent faire systématiquement rechercher une lésion de haut grade, masquée dans 15 à 30 % des cas. • La colposcopie est l’examen de référence, mais la difficulté est réelle quand la zone de jonction n’est pas vue ; on peut alors s’aider d’un curetage d’endocol ou d’un testing viral dont la valeur prédictive négative est très élevée, ce qui permet, en cas de négativité du test, de rassurer ces patientes ; la conisation diagnostique n’est pas recommandée sauf peut être au-delà de 45 ans. • La recherche d’HPV oncogènes dans l’exploration d’un frottis de bas grade n’a pas d’intérêt du fait de la forte prévalence des HPV oncogènes dans les lésions de bas grade. • Une fois le diagnostic retenu, il y a débat sur la gestion des CIN de bas grade : surveillance ou traitement ? Cela dépend de l’histoire naturelle, de l’âge, de la persistance, de la compliance , etc. • Globalement la régression est d’environ 50 % en moyenne entre 12 et 36 mois, ce qui est un plaidoyer pour l’abstention, sauf chez les patientes au-delà de 45 ans ou chez celles dont le suivi risque d’être problématique ou encore quand l’anomalie persiste au-delà de 18-24 mois. • En cas d’option thérapeutique, les traitements destructeurs ont la préférence, à la double condition que la colposcopie ne comporte aucun signe de « major change » et que la lésion soit observée dans sa totalité. • L’avenir est peut-être dans les techniques de génotypage en routine, permettant d’isoler dès le premier frottis de bas grade les patientes HPV 16 + qui sont à risque accru de lésion de haut grade et pour lesquelles un traitement anticipé pourrait être choisi, limitant le risque de perte de vue.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :





